Молекулска орбитала

У хемији, молекулска орбитала (скр. МО) је математичка функција која описује понашање електрона као таласа у молекулу.[1][2][3] Ова функција се може користити за израчунавање физичких и хемијских особина као што је налажење електрона у одређеном делу простора. Молекулске орбитале се најчешће конструишу комбинацијом атомских или хибридних орбитала сваког од атома у датом молекулу.[4][5] Термине атомска орбитала и молекуларна орбиталаШаблон:Efn увео је Роберт С. Маликен 1932. да означавају једноелектронске орбиталне таласне функције.[6] На елементарном нивоу, они се користе за описивање области простора у којој функција има значајну амплитуду.
На елементарном нивоу, молекулска орбитала се користи за описивање простора у коме функција има значајну амплитуду. У изолованом атому локација орбиталних електрона одређена је функцијама које се називају атомске орбитале. Када се више атома хемијски комбинује у молекул, локације електрона одређују молекул у целини, тако да се атомске орбитале комбинују и формирају молекуларне орбитале. Електрони из саставних атома заузимају молекуларне орбитале. Математички, молекуларне орбитале су приближно решење Шредингерове једначине за електроне у пољу атомских језгара молекула. Оне се обично граде комбинујући атомске орбитале или хибридне орбитале из сваког атома молекула или друге молекуларне орбитале из група атома. Оне се могу квантитативно израчунати помоћу Хартри-Фокововог или метода самоконзистентних поља (-{SCF}-).
Преглед
Молекуларна орбитала (МО) се може користити за представљање региона у молекулу где ће се вероватно наћи електрон који заузима ту орбиталу. Молекуларне орбитале су приближна решења Шредингерове једначине за електроне у електричном пољу атомских језгара молекула. Међутим, израчунавање орбитала директно из ове једначине је превише изазован проблем. Уместо тога, оне се добијају комбинацијом атомских орбитала, које предвиђају локацију електрона у атому. Молекулска орбитала може одредити електронску конфигурацију молекула: просторну дистрибуцију и енергију једног (или пара) електрона. Молекуларне орбитале се најчешће представљају као [[[Linear combination of atomic orbitals molecular orbital method|линеарна комбинација атомских орбитала]] (LCAO-MO метода), посебно у квалитативној или врло приближној употреби. Они су од непроцењиве вредности у пружању једноставног модела везивања у молекулима, схваћеног кроз молекуларну орбиталну теорију. Већина савремених метода у рачунарској хемији почиње израчунавањем молекулских орбитала система. Молекулска орбитала описује понашање једног електрона у електричном пољу које стварају језгра и неку просечну дистрибуцију осталих електрона. У случају да два електрона заузимају исту орбиталу, Паулијев принцип захтева да имају супротан спин. Ово је нужно апроксимација, а веома прецизни описи молекуларне електронске таласне функције немају орбитале (погледајте конфигурациону интеракцију).
Молекуларне орбитале су, генерално, делокализоване кроз цео молекул. Штавише, ако молекул има елементе симетрије, његове недегенерисане молекуларне орбитале су било симетричне или антисиметричне у односу на било коју од ових симетрија. Другим речима, примена операције симетрије S (нпр. рефлексија, ротација или инверзија) на молекуларну орбиталу ψ доводи до тога да молекуларна орбитала остане непромењена или да обрне свој математички предзнак: Sψ = ±ψ. У планарним молекулима, на пример, молекуларне орбитале су или симетричне (сигма) или антисиметричне (пи) у односу на рефлексију у молекуларној равни. Ако се узму у обзир и молекули са дегенерисаним орбиталним енергијама, важи општија тврдња да молекуларне орбитале формирају базе за несводљиве репрезентације групе симетрије молекула.[7] Својства симетрије молекуларних орбитала значе да је делокализација инхерентна карактеристика теорије молекуларних орбита и чини је фундаментално различитом од (и комплементарном) теорији валентне везе,[8][9] у којој се везе посматрају као локализовани електронски парови, уз узимање у обзир резонанције којом се објашњава делокализација.
За разлику од ових канонских молекуларних орбитала прилагођених симетрији, локализоване молекуларне орбитале могу се формирати применом одређених математичких трансформација на канонске орбитале.[10][11][12] Предност овог приступа је у томе што ће орбитале ближе одговарати „везама” молекула као што је приказано Луисовом структуром. Недостатак је да нивои енергије ових локализованих орбитала више немају физичко значење. (Дискусија у остатку овог чланка ће се фокусирати на канонске молекуларне орбитале. За даље дискусије о локализованим молекуларним орбиталама, погледајте: орбитала природне везе и сигма-пи и еквивалентни орбитални модели.)
Формирање молекуларних орбитала
Молекуларне орбитале настају из дозвољених интеракција између атомских орбитала, које су дозвољене ако су симетрије (утврђене из теорије група) атомских орбитала компатибилне једна са другом. Ефикасност атомских орбиталних интеракција се одређује на основу преклапања (мера колико добро две орбитале конструктивно интерагују једна са другом) између две атомске орбитале, што је значајно ако су атомске орбитале блиске по енергији. Коначно, број формираних молекуларних орбитала мора бити једнак броју атомских орбитала у атомима који се комбинују да би се формирао молекул.
Квалитативни опис
Све таласно механичке односно таласно механичке законитости које важе за атом, важе и за сложенији систем — молекул. То значи да су према овој теорији и методи електрони распоређени у молекулу као и у атому по одговарајућим орбиталама. Основна разлика је што су атомске орбитале моноцентричне, а молекулске су полицентричне тј. изграђују се око два или више атомских језгара.
Молекулске орбитале се могу добити методом линеарне комбинације атомских орбитала. Као резултат комбинације двије атомске орбитале, добијају се двије молекулске орбитале представљене збиром односно разликом атомских орбитала. Број молекулских орбитала које настају је једнак броју атомских орбитала које су укључене у линеарну комбинацију.[13]
При грађењу молекулске орбитале, у односу на атомску орбиталу долази до слиједећих промијена:
- губи се централна симетрија Кулоновског потенцијала (квантни број -{l}- више није добар квантни број за опис)
- електрони су истовремено придружени на оба атома
- долази до цијепања дегенерисаних енергетских нивоа
Линеарне комбинације атомских орбитала (LCAO)
Молекуларне орбитале су први увели Фридрих Хунд[14][15] и Роберт С. Муликен[16][17] 1927. и 1928. године.[18][19] Линеарну комбинацију атомских орбитала или „-{LCAO}-”[20][21] апроксимацију за молекуларне орбитале увео је 1929. године Џон Ленард-Џоунс.[22] Његов револуционарни рад показао је како се из квантних принципа може извести електронска структура молекула флуора и кисеоника. Овај квалитативни приступ молекуларно орбиталној теорији је део почетка модерне квантне хемије.
Линеарне комбинације атомских орбитала (-{LCAO}-) могу се користити за процену молекулских орбитала које настају везањем између саставних атома молекула. Слично атомској орбитали, Шредингерова једначина која описује понашање електрона такође се може конструисати за молекуларну орбиталу. Линеарне комбинације атомских орбитала, или збирови и разлике атомских таласних функција пружају приближна решења Хартри-Фокових једначина која одговарају апроксимацији независних честица молекуларне Шредингерове једначине. За једноставне дијатомске молекуле добијене таласне функције су математички представљене једначинама
где су и молекуларне таласне функције за везујуће и антивезујуће молекуларне орбитале, и су атомске таласне функције од атома а и б, а и су подесиви коефицијенти. Ови коефицијенти могу бити позитивни или негативни, зависно од енергије и симетрије појединих атомских орбитала. Како се два атома зближавају, њихове атомске орбитале се преклапају да би створиле подручја високе густине електрона, и као последица тога између два атома се формирају молекуларне орбитале. Атоми се држе заједно помоћу електростатичке привлачности између позитивно наелектрисаних језгара и негативно наелектрисаних електрона који заузимају везујуће молекуларне орбитале.[4]
Везујуће, антивезујуће и невезујући молекулске орбитале
Када атомске орбитале интерагују, резултујућа молекуларна орбитала може бити три типа: везујућа, антивезујућа или невезујућа.
- Интеракције везивања између атомских орбитала су конструктивне (у фази) интеракције.
- Везујуче МО имају нижу енергију од атомских орбитала које се комбинују да би их произвеле.
Антивезујуће молекулске орбитале:
- Интеракције против везивања између атомских орбитала су деструктивне (ван фазе) интеракције, са чворном равни где је таласна функција антивезујуће орбитале нула између два атома у интеракцији
- Антивезујуће МО имају више енергије од атомских орбитала које се комбинују да би их произвеле.
Невезујуће молекулске орбитале:
- Невезујуће МО су резултат одсуства интеракције између атомских орбитала због недостатка компатибилних симетрија.
- Невезујуће МО ће имати исту енергију као атомске орбитале једног од атома у молекулу.
Сигма и пи ознаке за молекулске орбитале
Тип интеракције између атомских орбитала може се даље категоризовати ознакама молекулско-орбиталне симетрије σ (сигма), π (пи), δ (делта), φ (фи), γ (гама) итд. Ово су кореспондирајућа грчка слова на атомске орбитале s, p, d, f и g, респективно. Број чворних равни које садрже међунуклеарну осу између дотичних атома је нула за σ МО, један за π, две за δ, три за φ и четири за γ.
σ симетрија
Молекулска орбитала са σ симетријом је резултат интеракције или две атомске s-орбитале или две атомске pz-орбитале. Молекулска орбитала ће имати σ-симетрију ако је орбитала симетрична у односу на осу која спаја два нуклеарна центра, међунуклеарну осу. То значи да ротација молекуларне орбитале око међунуклеарне осе не доводи до промене фазе. σ* орбитала, сигма антивезујућа орбитала, такође одржава исту фазу када се ротира око интернуклеарне осе. σ* орбитала има чворну раван која је између језгара и окомита је на међунуклеарну осу.[23]
π симетрија
Молекулска орбитала са π симетријом је резултат интеракције било две атомске px орбитале или py орбитале. Молекулска орбитала ће имати π симетрију ако је орбитала асиметрична у односу на ротацију око интернуклеарне осе. То значи да ће ротација молекулске орбитале око интернуклеарне осе довести до промене фазе. Постоји једна нодална раван која садржи међунуклеарну осу, ако се узму у обзир стварне орбитале.
π* орбитала, пи антивезујућа орбитала, такође ће произвести промену фазе када се ротира око интернуклеарне осе. π* орбитала такође има другу нодалну раван између језгара.[23][24][25][26]
δ симетрија
Молекулска орбитала са δ симетријом је резултат интеракције две атомске dxy или dx2-y2 орбитале. Пошто ове молекуларне орбитале укључују нискоенергетске d атомске орбитале, оне се виде у комплексима прелазних метала. δ везујућа орбитала има две нодалне равни које садрже међунуклеарну осу, а δ* антивезујућа орбитала такође има трећу нодалну раван између језгара.
φ симетрија
Шаблон:Further Шаблон:Multiple image
Теоретски хемичари су претпоставили да су везе вишег реда, као што су фи везе које одговарају преклапању f атомских орбитала, могуће. Не постоји познати пример молекула за који се тврди да садржи фи везу.
Парна и непарна симетрија
За молекуле који поседују центар инверзије (центросиметрични молекули[27][28]) постоје додатне ознаке симетрије које се могу применити на молекуларне орбитале. Центросиметрични молекули укључују:
- Хомонуклеарни дијатомици, X2
- Октаедарска, EX6
- Квадратна раван, EX4.
Нецентросиметрични молекули укључују:
- Хетеронуклеарни диатомици, XY
- Тетраедри, EX4.
Ако инверзија кроз центар симетрије у молекулу резултира истим фазама за молекуларну орбиталу, онда се каже да МО има џерајд (g) симетрију, од немачке речи за пар. Ако инверзија кроз центар симетрије у молекулу резултира променом фазе за молекуларну орбиталу, онда се каже да МО има анџерејд (u) симетрију, од немачке речи за непарно.
За везујућу молекулску орбиталу са σ-симетријом, орбитала је σg (s' + s'' је симетрична), док је антивезујућа молекулска орбитала са σ-симетријом орбитала σu, јер је инверзија s' – s'' антисиметрична.
За везујућу молекулску орбиталу са π-симетријом, орбитала је πu јер би инверзија кроз центар симетрије произвела промену знака (две p атомске орбитале су у фази једна са другом, али два режња имају супротне предзнаке), док је антивезујућа молекулска орбитала са π-симетријом πg јер инверзија кроз центар симетрије не би произвела промену знака (две p орбитале су антисиметричне по фази).[23]
Молекуларно орбитални дијаграми
Квалитативни приступ молекуларно орбиталне анализе користи молекуларни орбитални дијаграм за визуелизацију интеракција везивања у молекулу. У овом типу дијаграма, молекуларне орбитале су представљене хоризонталним линијама; што је линија веша то је енергија орбитале већа, а дегенерисане орбитале се постављају на исти ниво са размаком између њих. Затим, електрони који се постављају у молекуларне орбитале се постављају један по један, имајући на уму Паулијев принцип искључења и Хундово правило максималног мултиплицитета (само 2 електрона, који имају супротне спинове, по орбитали; стави се што више неспарених електрона на један ниво енергије пре него што се почне са упаривањем). За компликованије молекуле, таласно механички приступ губи корисност у квалитативном разумевању везивања (иако је и даље неопходан за квантитативни приступ).
Нека својства:
- Основни скуп орбитала укључује оне атомске орбитале које су доступне за молекуларне орбиталне интеракције, које могу бити везујуће или антивезујуће
- Број молекуларних орбитала једнак је броју атомских орбитала укључених у линеарну експанзију или базни скуп
- Ако молекул има неку симетрију, дегенерисане атомске орбитале (са истом атомском енергијом) се групишу у линеарне комбинације (које се називају атомске орбитале прилагођене симетрији (Шаблон:Јез-енг)), које припадају репрезентацији групе симетрије, те су таласне функције које описују групу познате као линеарне комбинације прилагођене симетрији (Шаблон:Јез-енг).
- Број молекуларних орбитала које припадају једној групној репрезентацији једнак је броју атомских орбитала прилагођених симетрији које припадају овој репрезентацији
- У оквиру одређене репрезентације, атомске орбитале прилагођене симетрији се више мешају ако су њихови атомски нивои енергије ближи.
Општи поступак за конструисање молекуларног орбиталног дијаграма за разумно једноставан молекул може се сажети на следећи начин:
- Доделите тачкасту групу молекулу.
- Потражите облике SALC-ова.
- Распоредите SALC-ове сваког молекуларног фрагмента по енергији, имајући у виду прво да ли потичу од s, p, или d орбитала (и ставите их у реду s < p < d), а затим по њиховом броју међунуклеарних чворова.
- Комбинујте SALC-ове истог типа симетрије из два фрагмента и од N SALC-ова формирајте N молекулских орбитала.
- Процените релативне енергије молекуларних орбитала из разматрања преклапања и релативне енергије матичних орбитала и нацртајте нивое на дијаграму нивоа молекуларне орбитале (који показује порекло орбитала).
- Потврдите, исправите и ревидирајте овај квалитативни поредак тако што ћете извршити прорачун молекуларне орбите помоћу комерцијалног софтвера.[29]
Везивање у молекулским орбиталама
Орбитална дегенерација
За молекуларне орбитале се каже да су дегенерисане ако имају исту енергију. На пример, у хомонуклеарним двоатомским молекулима првих десет елемената, молекуларне орбитале изведене из px и the py атомских орбитала доводе до две дегенерисане орбитале везе (ниске енергије) и две дегенерисане антивезујуће орбитале (високе енергије).[4]
Јонске везе
У јонској вези, супротно наелектрисани јони су повезани електростатичким привлачењем.[30] Могуће је описати јонске везе теоријом молекуларне орбите третирајући их као екстремно поларне везе. Њихове орбитале везивања су по енергији веома блиске атомским орбиталама анјона. Оне су такође по карактеру веома сличне атомским орбиталама анјона, што значи да су електрони потпуно померени ка анјону. У компјутерским дијаграмима, орбитале су центриране на анјонском језгру.[31]
Ред везе
Ред везе, или број веза, молекула може се одредити комбиновањем броја електрона у везујућим и антивезујућим молекуларним орбиталама. Пар електрона у орбитали везивања ствара везу, док пар електрона у антивезујућој орбитали негира везу. На пример, N2, са осам електрона у везујућим орбиталама и два електрона у антивезујућим орбиталама, има ред везе од три, што чини троструку везу.
Јачина везе је пропорционална реду везе – већа количина везивања производи стабилнију везу – а дужина везе је обрнуто пропорционална – јача веза је краћа.
Постоје ретки изузеци од захтева да молекул има позитиван ред везе. Иако Be2 има ред везе 0 према молекуларно орбиталноју анализи, постоје експериментални докази о веома нестабилном молекулу Be2 који има дужину везе од 245 pm и енергију везе од 10 kJ/mol.[23][32]
HOMO и LUMO
Највиша попуњена молекулска орбитала се назива -{HOMO}-, а најнижа молекулска орбитала која није попуњена се назива -{LUMO}-. Разлика између енергија -{HOMO}- и -{LUMO}- молекулских орбитала се назива забрањена зона и може да служи као мјера за способност побуђивања молекула, што је мања енергија то је молекул лакше побудити.
Номенклатура молекулских орбитала
При запису молекулских орбитала наводи сеШаблон:Sfn:
- атомске орбитале од којих потиче молекулска
- број чворних равни (број нодалних равни или равни симетрије) преко квантног броја λ
- да ли је орбитала везујућа или развезујућа
- симетрија орбитала (гераде -{g}- (од немачке речи за парно -{gerade}-) или унгераде -{u}- (непарно), у зависности од тога да ли је у односу на инверзију на центар симетрије орбитала парна или непарна)
Примери
-{H2}-

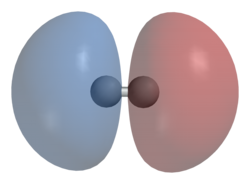
Молекул водоника се састоји од два атома водоника које означавамо са -{H'}- и -{H"}-. Линеарном комбинацијом -{1s'}- и -{1s"}- атомских орбитала добијају се две молекулске орбитале: једна везивна и друга антивезивна. Везивна молекулска орбитала се добије сабирањем атомских орбитала и одговара стању система у коме се електрон налази у везивној области. Антивезивна молекулска орбитала се односи на одузимање атомских орбитала и одговара стању система у коме се електрон налази у антивезивној области.
Везивна орбитала је по енергији нижа од атомских орбитала, док антивезивна орбитала има већу енергију.
Изградњу молекула од атома можемо описати прераспоређивањем електрона из атомских у молекулске орбитале.
У молекулу водоника имају два електрона при чему оба електрона се распоређују у везивну орбиталу при чему систем постаје нижи у енергији. При томе је направљена ковалентна веза.
Ред везе се дефинише као број електрона у везивним орбиталама минус број електрона у антивезивним орбиталама и све подијељено са два. У примјеру молекула водоника имају два електрона у везивној орбитали у нема електрона у антивезивним орбиталама, па је ред везе један и постоји једна веза између атома водоника.
-{He2}-
Хелијум има два електрона у -{1s}- орбитали у основном стању. У случају хипотетичког молекула -{He2}-, два електрона би попунила везивну орбиталу а два антивезивну и резултујућа електронска густина не подржава формирање везе између атома и молекул не постоји. Ред везе је нула и веза не постоји.
Да би могла да се успостави хемијска веза тј. награди молекул једињења потребно је да број електрона у везивним орбиталама буде већи него у антивезивним.
Молекул -{HeH}- би имао мало мању енергију него почетни атоми, али већу енергетску предност тј. мању енергију има -{H2 + 2 He}-, тако да молекул -{HeH}- постоји само кратко.
Li2
Дилитијум Li2 се формира преклапањем 1s и 2s атомских орбитала (базни скуп) два Li атома. Сваки атом Li доприноси са три електрона интеракцијама везивања, а шест електрона испуњава три молекулске орбитале најниже енергије, σg(1s), σu*(1s), и σg(2s). Користећи једначину за ред везе, утврђено је да дилитијум има ред везе од један, једноструке везе.[33]
Племенити гасови
Узимајући у обзир хипотетички молекул He2 пошто је основни скуп атомских орбитала исти као у случају of H2, налази се да су везујуће и антивезујуће попуњене, тако да нема енергетске предности за формирање пара. HeH би имао благу енергетску предност, али не толико као H2 + 2 He, тако да је молекул веома нестабилан и постоји само кратко пре него што се распадне на водоник и хелијум. Генерално, налазимо да се атоми као што је He који имају пуне енергетске љуске ретко везују за друге атоме. Осим краткотрајних Ван дер Валсових комплекса, врло је мало једињења племенитих гасова познато.[34][35][36][37]
Хетеронуклеарни диатомици
Док молекулске орбитале за хомонуклеарне двоатомске молекуле садрже једнаке доприносе сваке атомске орбитале у интеракцији, МО за хетеронуклеарне диатоме садрже различите атомске орбиталне доприносе. Орбиталне интеракције за продукцију везивања или антивезивања орбитала у хетеронуклеарним диатомицима се дешавају ако постоји довољно преклапања између атомских орбитала што је одређено њиховим симетријама и сличношћу у орбиталним енергијама.
HF
У флуороводонику HF преклапање између H 1s и F 2s орбитала је дозвољено симетријом, али разлика у енергији између две атомске орбитале спречава их да интерагују како би се створила молекуларна орбитала. Преклапање између H 1s и F 2pz орбитала је такође симетријски дозвољено, и ове две атомске орбитале имају мало енергетско раздвајање. Стога, оне формирају интеракције, што доводи до стварања σ и σ* МО и молекула са редом везе од 1. Пошто је HF нецентросиметричан молекул, ознаке симетрије g и u нису применљиве на његове молекуларне орбитале.[38]
Квантитативни приступ
Да би се добиле квантитативне вредности за молекуларне нивое енергије, потребно је да постоје молекуларне орбитале које су такве да експанзија конфигурационе интеракције[39][40] брзо конвергира ка лимиту пуне конфигурационе интеракције.[41][42] Најчешћи метод за добијање таквих функција је Хартри–Фоков метод, који изражава молекуларне орбитале као сопствене функције Фоковог оператора. Обично се овај проблем решава проширењем молекуларних орбитала као линеарних комбинација Гаусових функција центрираних на атомским језгрима (види линеарну комбинацију атомских орбитала и хемијски базни сет[43][44][45]). Једначине за коефицијенте ових линеарних комбинација су генерализоване једначине сопствених вредности познате као Рутанове једначине,[46][47][48] које су заправо посебан приказ Хартри–Фокове једначине. Постоји велики број програма у којима се могу извршити квантно хемијски прорачуни МО, укључујући Спартан.[49][50][51][52][53][54]
Једноставни прорачуни често сугеришу да се експерименталне молекуларне орбиталне енергије могу добити методама ултраљубичасте фотоелектронске спектроскопије за валентне орбитале и рендгенске фотоелектронске спектроскопије за сржне орбитале. Ово, међутим, није тачно јер ови експерименти мере енергију јонизације, разлику у енергији између молекула и једног од јона, која је резултат уклањања једног електрона. Енергије јонизације су приближно повезане са орбиталним енергијама Купмансовом теоремом.[55][56][57][58][59] Док сагласност између ове две вредности може бити блиска за неке молекуле, у другим случајевима може бити веома лоша.
Енергетски дијаграми
У случају сложенијих молекула, таласно механички модел је погодан за квантитивни опис веза, али не и за квалитативни. Због тога се уводе енергетски дијаграми у којима се молекулске орбитале представљене хоризонталним линијама, при чему орбитале које имају вишу енергију су нацртане више. Дегенерисане орбитале (орбитале са истом енергијом) су представљене на истом нивоу, али се између њих налази размак. Електрони се попуњавају један по један придржавајући се Паулијевог принципа искључења и Хундовог правила тј. у једној орбитали се налазе максимално два електрона супротног спина, на истом енергетском нивоу електрони се попуњавају да има максималан број неспарених електрона а затим се упарују.

Види још
Напомене
Референце
Литература
- Шаблон:Cite book
- Шаблон:Cite book
- Шаблон:Cite book
- Шаблон:Cite book
- Шаблон:Cite book
- Шаблон:Cite book
- Шаблон:Cite book
- Quantum degeneracy in two dimensional systems, Debnarayan Jana, Dept. of Physics, University College of Science and Technology
- Шаблон:Cite book
- Orchin, M. Jaffe, H.H. (1967) The Importance of Antibonding Orbitals. Houghton Mifflin. ISBN B0006BPT5O
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
- Шаблон:Cite journal
Спољашње везе
- -{Java molecular orbital viewer shows orbitals of hydrogen molecular ion.}-
- Шаблон:Cite web Шаблон:Wayback, a visualization of all atomic, and some molecular and hybrid orbitals}-
- -{xeo Visualizations of some atomic and molecular atoms}-
Шаблон:Хемијске везе Шаблон:Нормативна контрола
- ↑ Peter Atkins; Julio De Paula. Atkins’ Physical Chemistry. Oxford University Press. 8th ed., 2006.}-
- ↑ -{Yves Jean; Francois Volatron. An Introduction to Molecular Orbitals. Oxford University Press, 1993.}-
- ↑ Шаблон:Harvnb
- ↑ 4,0 4,1 4,2 Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ F. Hund, "Zur Deutung der Molekelspektren", Zeitschrift für Physik, Part I, vol. 40, pages 742-764 (1927); Part II, vol. 42, pages 93–120 (1927); Part III, vol. 43, pages 805-826 (1927); Part IV, vol. 51, pages 759-795 (1928); Part V, vol. 63, pages 719-751 (1930).
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Friedrich Hund and Chemistry, Werner Kutzelnigg, on the occasion of Hund's 100th birthday, Angewandte Chemie International Edition, 35, 573–586, (1996)
- ↑ Robert S. Mulliken's Nobel Lecture, Science, 157, no. 3785, 13-24. Available on-line at: Nobelprize.org
- ↑ Huheey, James. Inorganic Chemistry:Principles of Structure and Reactivity
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ 23,0 23,1 23,2 23,3 Catherine E. Housecroft, Alan G. Sharpe, Inorganic Chemistry, Pearson Prentice Hall; 2nd Edition, 2005, p. 29-33.
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite web
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite web
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Catherine E. Housecroft, Alan G, Sharpe, Inorganic Chemistry, Pearson Prentice Hall; 2nd Edition. Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book. John Wiley and Sons.
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite book
- ↑ Шаблон:Cite journal
- ↑ Шаблон:Cite journal
- ↑ See, for example, Шаблон:Cite book